Soal pilihan Ganda tentang Sifat Koligatif Larutan
Kompetensi Dasar
Indikator
- Menjelaskan penurunan tekanan uap, kenaikan titik didih, penurunan titik beku larutan, dan tekanan osmosis termasuk sifat koligatif larutan.
- Membandingkan antara sifat koligatif larutan non elektrolit dengan sifat koligatif larutan elektrolit yang konsentrasinya sama berdasarkan data percobaan.
Indikator
- Menghitung konsentrasi suatu larutan (kemolalan dan fraksi mol
- Menjelaskan pengertian sifat koligatif larutan non elektrolit (hukum Roulth) dan larutan elektrolit
- Menjelaskan pengaruh zat terlarut yang sukar menguap terhadap tekanan uap pelarut.
- Menghitung tekanan uap larutan berdasarkan data percobaan.
- Mengamati penurunan titik beku suatu zat cair akibat penambahan zat terlarut melalui percobaan
- Menghitung penurunan titik beku larutan elektrolit dan non elektrolit berdasarkan data percobaan
- Mengamati kenaikan titik didih suatu zat cair akibat penambahan zat terlarut melalui percobaan
- Menghitung kenaikan titik didih larutan elektrolit dan non elektrolit berdasarkan data percobaan
- Menganalisis diagram PT untuk menafsirkan penurunan tekanan uap, penurunan titik beku dan kenaikan titik didih larutan
- Menjelaskan pengertian osmosis dan tekanan osmosis serta terapannya
- Menghitung tekanan osmosis larutan elektrolit dan non elektrolit
- Menganalisis data percobaan untuk membandingkan sifat koligatif larutan elektrolit dan non elektrolit
Pilihlah Jawaban Yang Tepat
Soal 1
Molalitas larutan NaCl 10% massa dalam air adalah . . . . .m (Mr NaCl = 58,5)
A. 1,50
B. 1,70
C. 1,90
D. 2,10
E. 2,30
Soal 2
Sebanyak 30 gram urea dilarutkan dalam 81 gram air akan menghasilkan larutan dengan fraksi mol sebesar . . . . .(Mr Urea = 60,Mr 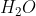 = 18).
= 18).
A. 0,10
B. 0,11
C. 0,45
D. 0,50
E. 0,88
Soal 3
Molalitas larutan etanol yang mempunyai 35 % massa dalam air adalah . . . .m(Ar H = 1, C = 12, O = 16).
A. 8,7
B. 9,7
C. 10,7
D. 11,7
E. 12,7
Soal 4
Fraksi mol zat terlarut dan pelarut jika ke dalam 90 gram air dilarutkan 18 gram glukosa secara berturut utrut adalah . . . .
A. 0,01 dan 0,02
B. 0,02 dan 5
C. 0,01 dan 0,98
D. 0,02 dan 0,98
E. 0,02 dan 0,99
Soal 5
A. 6,4
B. 5,4
C. 4,4
D. 3,4
E. 0,4
Soal 6
Larutan berikut yang memiliki titik beku tertinggi adalah . . . . .
A. Glukosa 0,05 M
B. Glukosa 0,10 M
C. Sukrosa 0,10 M
D. Sukrosa 0,15 M
E. Urea 0,15 M
Soal 7
Kenaikan titik didih molal bergantung pada . . . . .
A. Jenis pelarut
B. Titik didh Pelarut
C. Molaritas larutan
D. Molalitas larutan
E. Jenis za terlarut
Soal 8
Jika diketahui derajar ionisasi 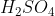 dalam larutan = 1 dan Kb air =
dalam larutan = 1 dan Kb air =  , kenaikan titik didih larutan 24,5 gram
, kenaikan titik didih larutan 24,5 gram 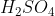 (Mr = 98) dalam 250 gram air sebesar . . . . .
(Mr = 98) dalam 250 gram air sebesar . . . . .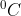
A. 0,13
B. 0,39
C. 0,52
D. 0,72
E. 1,56
Soal 9
A. 2,4
B. 4,3
C. 6,0
D. 7,2
E. 8,4
Soal 10
Perhatikan diagram P - T!
A. K - L
B. K - R
C. M - N
D. T - M
E. T - R
Soal 11
Perhatikan gambar beberapa larutan di bawah ini!
Jika volume larutan semua larutan tersebut dianggap sama, larutan ynag mempunyai tekanan osmotik paling rendah saat diukur pada suhu tetap dan R = 0,082 adalah larutan . . . . .
A. P
B. Q
C. R
D. S
E. T
Soal 12
Ke dalam 500 gram air dilarutkan 40 gram senyawa _{3}) . Jika Kb air =
. Jika Kb air =  , derajat ionisasi 0,8, kenaikan titik didih larutan tersebut adalah . . . . .
, derajat ionisasi 0,8, kenaikan titik didih larutan tersebut adalah . . . . .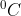 (Ar Fe = 56, S = 32, O = 18)
(Ar Fe = 56, S = 32, O = 18)
A. 0,333
B. 0,354
C. 0,416
D. 0,437
E. 0,496
Soal 13
Sebanyak 12 gram NaCl dilarutkan dalam 600 mL larutan. Jika diketahui NaCl terionisasi 80 % pada suhu  , Larutan tersebut mempunyai tekanan osmotik sebesar . . . .atm.
, Larutan tersebut mempunyai tekanan osmotik sebesar . . . .atm.
(R = 0,082 L atm /mol K, Ar Na = 23, Cl = 35,5)
A. 12,14
B. 13,14
C. 14,14
D. 15,14
E. 16,14
Soal 14
Dalam 300 gram air terlarut 40 gram zat X. Larutan tersebut membeku pada suhu  . Jika Kf air =
. Jika Kf air = , Mr zat X tersebut adalah . . . . .
, Mr zat X tersebut adalah . . . . .
A. 30
B. 40
C. 46
D. 60
E. 80
Soal 15
Berikut ini dalam kehidupan sehari hari
- Etilen glikol ditambahin ke dalam radiator mobil
- Destilasi air laut
Kedua contoh soal diatas berhubungan dengan sifat koligatif larutan secara berturut turut . . . . .
A. Penurunan tekanan uap dan tekanan osmotik
B. Tekanan osmotik dan kenaikan titik didih
C. Kanikan titik didh dan penurunan titik beku
D. Penurunan titik beku dan osmotik balik
E. Penurunan titik beku dan kenaikan titik didih
Soal 16
Larutan 3 gram glukosa (Mr = 180) dalam 250 mL air isotonik dengan larutan 4,6 gram X dalam 500 mL air. Zat X tersebut memiliki massa molekul relatif . . . . .
A. 69
B. 138
C. 276
D. 342
E. 684
Soal 17
Larutan 7,6 gram kamfer (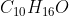 ) dalam 400 gram kloroform (
) dalam 400 gram kloroform ( ) memiliki titik didih
) memiliki titik didih  lebih tinggi dari titik didih kloroform murni. Tetapan titik didih molal kloroform adalah . . . . .
lebih tinggi dari titik didih kloroform murni. Tetapan titik didih molal kloroform adalah . . . . .
A. 0,48
B. 1,84
C. 2,48
D. 3,84
E. 5,44
Soal 18
Suatu larutan glukosa (Mr = 180) dalam 2 kg air (Kb = 0,52) ternyata mendidih pada suhu  . Massa glukosa yang dilarutkan adalah . . . . .gram.
. Massa glukosa yang dilarutkan adalah . . . . .gram.
A. 245
B. 450
C. 502
D. 547
E. 695
Soal 19
Suatu larutan terdiri atas 12 gram zat X (non elektrolit) di dalam 20 gram air. Jika larutan membeku pada suhu  dan penurunan titik beku molal air
dan penurunan titik beku molal air , zat X tersebut mempunyai massa molekul relatif . . . . .
, zat X tersebut mempunyai massa molekul relatif . . . . .
A. 59
B. 118
C. 223
D. 277
E. 336
Soal 20
Sebanyak 37 gram dilarutkan ke dalam 250 gram air. Larutan tersebut mendidih pada suhu  . Jika Ar : Ca = 40, O = 16, H = 1, dan Kb air =
. Jika Ar : Ca = 40, O = 16, H = 1, dan Kb air = , derajat ionisasi basa tersebut sebesar . . . . .%
, derajat ionisasi basa tersebut sebesar . . . . .%
A. 85
B. 75
C. 65
D. 55
E. 45
Soal 21
Sebanyak 1 mol gula dilarutkan ke dalam 100 gram air, mendidih pada suhu  . Untuk suatu larutan alkohol, agar mendidih pada suhu yang sama dengan larutan gula, dalam 100 gram air dilarutkan alkohol sebanyak . . . . mol
. Untuk suatu larutan alkohol, agar mendidih pada suhu yang sama dengan larutan gula, dalam 100 gram air dilarutkan alkohol sebanyak . . . . mol
A. 1,00
B. 0,50
C. 0,20
D. 0,05
E. 0,10
Soal 22
Tekanan uap air jenuh pada suhu  adalah 31,8 mmHg dan fraksi mol suatu zat dalam air 0,056 mol. Pada suhu
adalah 31,8 mmHg dan fraksi mol suatu zat dalam air 0,056 mol. Pada suhu  tekanan uap larutan adalah . . . . .mmHg.
tekanan uap larutan adalah . . . . .mmHg.
A. 1,78
B. 17,8
C. 28,30
D. 30,02
E. 33,58
Soal 23
Sebanyak 18 gram glukosa dimasukkan ke dalam 500 gram air. Jika kalor beku molal air, Kf =  , titik beku larutan tersebut adalah . . . . .
, titik beku larutan tersebut adalah . . . . .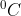 (Ar C = 12, H = 1, O =16)
(Ar C = 12, H = 1, O =16)
A. - 0,18
B. - 0,36
C. - 1,8
D. - 3,6
E. - 7,2
Soal 24
Berikut ini jumlah pertikel zat terlarut yang terdapat dalam 2 mol pelarut dalam ruang tertutup.
A. 1
B. 2
C. 3
D. 4
E. 5
Soal 25
Tabel berikut menunjukkan data sejumlah zat telarut yang dilarutkan dalam air.
Jika R = 0,082 L atm/mol K dan pengukuran dilakukan pada suhu tetap, larutan yang mempunyai tekanan osmotik paling besar adalah . . . . .
A. 1
B. 2
C. 3
D. 4
E. 5
Soal 26
Sebanyak 4 gram zat X dilarutkan dalam 5.000 mL larutan benzena yang diketahui mempunyai tekanan 19 mmHg. Jika larutan tersebut diukur pada keadaan yang sama saat 6 gram zat X dilarutkan dalam 12 liter gas etana pada tekanan 38 cmHg, massa molekul relatif zat X tersebut adalah . . . . .
A. 136
B. 125
C. 112
D. 100
E. 96
Soal 27
Kenaikan titik didih larutan sama dengan Kb apabila . . . . .
A. Molalitas larutan = 1 molal
B. Molaritas larutan = 1 molar
C. Fraksi mol larutan = 1
E. Kf air = 1
Soal 28
Dikeathui beberapa larutan berikut.
Berdasarkan data diatas, larutan yang mepunyai kesamaan titik beku ditunjukkan oleh nomor . . . . .
A. 1 dan 2
B. 1 dan 3
C. 2 dan 3
D. 2 dan 4
E. 3 dan 4
Soal 29
Suatu elektrolit kuat bermassa 18,8 gram dilarutkan kedalam 200 gram air (Kb = ). Titik didih larutan ynag terjadi yaitu
). Titik didih larutan ynag terjadi yaitu  . Jika faktor Van't Hoff = 3 dan derajat ionisasi = 1, senyawa tersebut adalah . . . . .(Ar H = 1, S = 32, O =16, N =14, Na = 23, Ca = 40, Cl = 35,5, Ba = 137,327)
. Jika faktor Van't Hoff = 3 dan derajat ionisasi = 1, senyawa tersebut adalah . . . . .(Ar H = 1, S = 32, O =16, N =14, Na = 23, Ca = 40, Cl = 35,5, Ba = 137,327)
C. NaOH
Soal 30
Penurunan titik beku dan kenaikan titik didih larutan garam 1 molal lebih besar daripada larutan gula 1 molal. Hal ini disebabkan . . . .
A. Jumlah atom dalam larutan garam lebih sedikit daripada larutan gula.
B. Kedua larutan mempunyai harga molalitas yang sama
C. Garam merupakan larutan nonelektrolit
D. Mr garam lebih kecil daripada Mr gula
E. Garam merupakan larutan elektrolit





Posting Komentar untuk "Soal pilihan Ganda tentang Sifat Koligatif Larutan"