Macam Macam Cara Identifikasi Karbohidrat
Identifikasi karbohidrat maksudnya adalah menguji suatu zat apakah mengandung karbohidrat atau tidak. Melalui beberapa percobaan berikut kita bisa mengidentifikasi ada atau tidaknya karbohidrat dalam suatu zat .
Percobaan ini pertama kali dilakukan oleh seorang botanis Austria bernama Hans Molisch. Percobaan ini betujuan untuk mengidentifikasi adanya karbohidrat dalam suatu zat dengan prinsip percobaan adalah mendehidrasi karbohidrat dengan asam sulfat atau asam klorida untuk menghasilkan senyawa aldehida.
Senyawa aldehida ini akan terkondensasi dengan dua molekul fenol (biasanya adalah alfa-naftol yang ada dalam reagen molis) menghasilkan cincing berwarna merah atau ungu di bagian bawah tabung.
Reaksi yang terjadi adalah sebagai berikut :
Alfa – naftol berfungsi sebagai insikator warna sedangkan H2SO4 atau asam klorida berfungsi untuk menghidrolisis :
Glukosa (heksosa => mengandung 6 C) ==> hidroksi metil furfural
Arabinosa (pentosa = yang mengandung 5 C) ==> furfural.
Reaksi uji Molisch positif untuk semua karbohidrat, jadi ini adalah test umum yang digunakan untuk mengidentifikasi ada atau tidaknya karbohidrat dalam suatu zat.
Dalam uji ini, zat akan direaksikan dengan reagen Selliwanof yang terdiri dari campuran 0,5 % senyawa 1,3 – dihidroksi benzene (resorsinol) dan HCl encer. Uji positif adanya gugus keton ditandai dengan terbentuknya warna merah. HCl berfungsi untuk menghidrolisis fruktosa (atau ketosa) menjadi hidroksi metil furfural yang kemudian akan membentuk kompleks berwarna merah dengan resorsinol (1,3 – dihidroksi benzena).
Kenapa digunakan HCl encer? Alasannya adalah mungkin saja dalam zat juga terdapat senyawa aldosa (karbohidrat dengan gugus aldehid). Aldosa bisa terhidrolisis banyak hanya dengan asam pekat sementara ketosa bisa kita hidrolisis hanya dengan asam encer. Digunakan HCl encer agar ketosa nya yang terlebih dahulu terhidrolisis kemudian membentuk kompleks dengan resorsinol.
Uji seliwanof juga bisa kita lakukan pada disakarida yang mengandung fruktosa seperti sukrosa. Sukrosa akan terhidrolisis menjadi glukosa dan fruktosa. Dalam HCl encer, yang akan terhidrolisis terlebih dahulu menjadi hidroksi metil furfural adalah fruktosanya sedangkan glukosa butuh asam pekat agar terhidrolisis lebih banyak. Akibatnya fruktosalah yang bereaksi dengan resorsinol membentuk kompleks berwarna merah.
Jika kita lakukan uji pada maltosa misalnya, ma aia kan menunjukkan hasil negative. Hal ini disebabkan karena maltosa terhidrolisis menghasilkan dua buah molekul glukosa yang kurang reaktif terhadap HCl encer.
Uji ini hanya berlaku untuk polisakarida, tidak untuk monosakarida ataupun disakarida. Hal ini disebabkan karena molekulnya masih sederhana.
Amilum termasuk polisakarida yang dapat mengalami hidrolisis. Hidrolisis amilum menjadi disakarida dan monosakarida berlangsung beberapa tahap. Dengan menggunakan ion kita bisa mengatahui tahap apa saja yang dialami amilum saat terhidrolisis.
Pada percobaan ini, amilum akan diireaksikan dengan HCl kemudian dipanaskan. Maka amilum akan terhidrolisis melalui tahan tahap berikut :
Amilum Amilo Eritro Akroo
+ HCl => dekstrin => dekstrin =>dekstrin => Maltosa => Glukosa
+ + + + + +
Iod Iod Iod Iod Iod Iod
| | |
Biru Ungu Merah Tidak Berwarna
Reagen bennedict terdiri dari :
Glukosa + reagen Bennedict ===> enol reaktif
∆
Enol reaktif + Cu2+ ==> Cu+
Cu+ akan bereaksi dengan OH- menbentuk CuOH yang berwarna kuning. Dengan pemanansan akan berubah menjadi endapan Cu2O.
Cu+ + OH- ==> CuOH (kuning) ===> Cu2O
∆
Endapan yang dihasilkan memiliki warna yang tergantung pada jumlah Cu2O yang terbentuk. Ada warna hijau, kuning, orange, merah sampai merah bata. Oleh karena itu, uji Bennedict bisa digunakan sebagai uji kualitatif maupun kuantitatif.
Oleh karena itu pembentukan osazon menjadi begitu penting karena selain dapat digunakan mengidentifikasi karbohidrat, juga bisa digunakan untukmembedakan beberapa karbohidrat dengan mengidentifikasi konfigurasi strukturalnya.
Glukosa dan fruktosa memberikan osazon yang sama karena kedua monosakarida tersebut memiliki gugus H dan OH yang terletak pada atom C yang sama yaitu atom C ke 3, 4 dan 5. Manosa tidak membentuk osazon melainkan membentuk fenilhidrazon yang tidak larut.
Semua disakarida kecuali sukrosa tidak membentuk osazon.
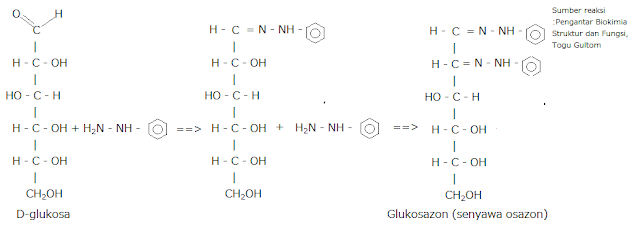
Berikut reaksi pembentukan osazon :
Furfural yang terbentuk akan bereaksi dengan benzidin membentuk kompleks senyawa berwarna merah anggur.
Reaksi yang terjadi adalah sebagai berikut :
1. Pentosa (arabinosa) + CH3COOH glacial ==> furfural + 3H2O
∆
2. Furfural + benzidin ==> senyawa kompleks yang berwarna merah anggur
Untuk melakukannya, dibutuhkan dua buah tabung reaksi. Didalam tabung reaksi ini masing-masing dimasukkan sukrosa. Kemudian dalam kedua tabung dimasukkan HCl, reagen Bennedict dan timol biru. HCl berfungsi sebagai penghidrolisis sukrosa sedangkan timol birunya berfungsi sebagai indicator.
Reagen Bennedict berfungsi sebagai penanda putusnya ikatan monosakarida dalam sukrosa. Sukrosa akan dihidrolisis menjadi fruktosa dan glukosa dimana glukosa akan bereaksi positif menghasilkan endapan merah bata. Artinya jika ada endapan merah bata maka sukrosanya telah terhidrolisis.
Tabung I akan dipanaskaskan sedangkan tabung II tidak. Tabung yang dipanaskan akan terjadi reaksi hidrolisis sukrosa sementara tabung dua tidak. Seperti yang dijelaskan diatas bahwa pada tabung I akan terbentuk endapan merah bata yang menandai telah putusnya ikatan diantara fruktosa dan glukosa yang membentuk disakarida.
Jika ada amilum dalam zat tersebut, maka kelarutannya akan berkurang dan akhirnya mengendap. Larutan amilum dan ammonium sulfat jenuh yang dipanaskan akan menghasilkan endapan berwarna putih.
Metode ini juga bisa digunakan untuk memisahkan amilum dari larutan. Amilum yang mengendap ada dalam jumlah yang banyak, sedangkan filtratnya hanya mengandung sedikit amilum. Dengan menyaring, kita bisa mendapatkan amilum padat. Sementara amilum yang masih ada dalam flitrat dapat kita endapkan terus melalui cara diatas sampai amilumnya habis. Hal ini bisa ditandai dengan tidak terbentuknya warna biru jika filtratrnya ditetesi iod.
Sama dengan karbohidrat lain, untuk menghidrolisis gom arab digunakan HCl dan dilakukan pemanasan. Setelah beberapa saat pemanasan, kita akan menghentikan proses hidrolisis yaitu dengan caramendinginkannya dan menambah NaOH agar suasana larutan menjadi netral.
Gula pentosa (arbinosa) yang dihasilkan dari proses hidrolisis akan bereaksi positif dengan reagen Tauber menghasilkan larutan berwarna merah. Selain itu arabinosa juga akan menghasilkan endapat merah bata yang menandai bahwa ia adalah gula pereduksi (yang memiliki gugus karbonil bebas).
Sumber :
1.Bahan ajar biokimia, poltekes bengkulu, 2011
2. Pengantar biokimia, fungsi dan struktur. Togu gultom,2001 . Fakultas pendidikan Kimia . UNY
3. Buku PR kimia kelas 12 SMA, Penerbit intan pariwara
4. Pengantar biokimia, togu gultom, fakultas pendidikan kimia, universitas yogyakarta.
Penulis: Ririn Nababan
Percobaan Molisch
Percobaan ini pertama kali dilakukan oleh seorang botanis Austria bernama Hans Molisch. Percobaan ini betujuan untuk mengidentifikasi adanya karbohidrat dalam suatu zat dengan prinsip percobaan adalah mendehidrasi karbohidrat dengan asam sulfat atau asam klorida untuk menghasilkan senyawa aldehida.
Senyawa aldehida ini akan terkondensasi dengan dua molekul fenol (biasanya adalah alfa-naftol yang ada dalam reagen molis) menghasilkan cincing berwarna merah atau ungu di bagian bawah tabung.
Reaksi yang terjadi adalah sebagai berikut :
 |
| Reaksi uji Molisch. Image from wikipedia.org |
Glukosa (heksosa => mengandung 6 C) ==> hidroksi metil furfural
Arabinosa (pentosa = yang mengandung 5 C) ==> furfural.
Reaksi uji Molisch positif untuk semua karbohidrat, jadi ini adalah test umum yang digunakan untuk mengidentifikasi ada atau tidaknya karbohidrat dalam suatu zat.
Uji Selliwanof
Reaksi Selliwanof adalah reaksi yang bertujuan untuk mengidentifikasi adanya gugus keton pada suatu disakarida. Reaksi ini juga sring disebut sebagai reaksi uji fruktosa (karena mengandung gugus keton).Dalam uji ini, zat akan direaksikan dengan reagen Selliwanof yang terdiri dari campuran 0,5 % senyawa 1,3 – dihidroksi benzene (resorsinol) dan HCl encer. Uji positif adanya gugus keton ditandai dengan terbentuknya warna merah. HCl berfungsi untuk menghidrolisis fruktosa (atau ketosa) menjadi hidroksi metil furfural yang kemudian akan membentuk kompleks berwarna merah dengan resorsinol (1,3 – dihidroksi benzena).
Kenapa digunakan HCl encer? Alasannya adalah mungkin saja dalam zat juga terdapat senyawa aldosa (karbohidrat dengan gugus aldehid). Aldosa bisa terhidrolisis banyak hanya dengan asam pekat sementara ketosa bisa kita hidrolisis hanya dengan asam encer. Digunakan HCl encer agar ketosa nya yang terlebih dahulu terhidrolisis kemudian membentuk kompleks dengan resorsinol.
Uji seliwanof juga bisa kita lakukan pada disakarida yang mengandung fruktosa seperti sukrosa. Sukrosa akan terhidrolisis menjadi glukosa dan fruktosa. Dalam HCl encer, yang akan terhidrolisis terlebih dahulu menjadi hidroksi metil furfural adalah fruktosanya sedangkan glukosa butuh asam pekat agar terhidrolisis lebih banyak. Akibatnya fruktosalah yang bereaksi dengan resorsinol membentuk kompleks berwarna merah.
Jika kita lakukan uji pada maltosa misalnya, ma aia kan menunjukkan hasil negative. Hal ini disebabkan karena maltosa terhidrolisis menghasilkan dua buah molekul glukosa yang kurang reaktif terhadap HCl encer.
Percobaan Iod – Uji polisakarida
Amilum adalah polisakarida yang memiliki struktur spiral (menutup) dan jika kita masukkan iod ke dalam polisakarida itu, maka molekul iod akan terperangkap didalamnya menghasilkan larutan berwarna tertentu seperti amilum akan berwarna biru sedangkan glikogen berwarna coklat.Uji ini hanya berlaku untuk polisakarida, tidak untuk monosakarida ataupun disakarida. Hal ini disebabkan karena molekulnya masih sederhana.
Uji amilum
Amilum termasuk polisakarida yang dapat mengalami hidrolisis. Hidrolisis amilum menjadi disakarida dan monosakarida berlangsung beberapa tahap. Dengan menggunakan ion kita bisa mengatahui tahap apa saja yang dialami amilum saat terhidrolisis.
Pada percobaan ini, amilum akan diireaksikan dengan HCl kemudian dipanaskan. Maka amilum akan terhidrolisis melalui tahan tahap berikut :
Amilum Amilo Eritro Akroo
+ HCl => dekstrin => dekstrin =>dekstrin => Maltosa => Glukosa
+ + + + + +
Iod Iod Iod Iod Iod Iod
| | |
Biru Ungu Merah Tidak Berwarna
Uji Bennedict
Reaksi Bennedict adalah reaksi untuk menguji adanya gugus karbonil bebas (aldehid). Reaksi ini positif untuk semua monosakarida dan disakarida kecuali sukrosa. Prinsip uji ini adalah adanya reaksi redoks dimana gula yang mengandung gugus karbonil bebas dapat mereduksi reagen Bennedict.Reagen bennedict terdiri dari :
- CuSO4 yang berfungsi sebagai penyedia ion Cu2+
- Natrium sitrat yang berfungsi sebagai penghambat terbentuknya endapan Cu(OH)2 atau CuCO3¬.
- Na2CO3 yang berfungsi untuk mengubah gugus arbonil karbohidrat menjadi bentuk enol reaktif.
Glukosa + reagen Bennedict ===> enol reaktif
∆
Enol reaktif + Cu2+ ==> Cu+
Cu+ akan bereaksi dengan OH- menbentuk CuOH yang berwarna kuning. Dengan pemanansan akan berubah menjadi endapan Cu2O.
Cu+ + OH- ==> CuOH (kuning) ===> Cu2O
∆
Endapan yang dihasilkan memiliki warna yang tergantung pada jumlah Cu2O yang terbentuk. Ada warna hijau, kuning, orange, merah sampai merah bata. Oleh karena itu, uji Bennedict bisa digunakan sebagai uji kualitatif maupun kuantitatif.
Reaksi fenilhidrazin (pembentukan osazon)
Osazon terbentuk ketika karbohidat yang memiliki gugus aldehid atau keton bebas bereaksi dengan fenilhidrazin. Osazon adalah senyawa yang tidak larut dalam air dan membentuk kristal. Kristal yang dihasilkan ini memiliki bentuk yang spesisfik sesuai dengan jenis karbohidratnya.Oleh karena itu pembentukan osazon menjadi begitu penting karena selain dapat digunakan mengidentifikasi karbohidrat, juga bisa digunakan untukmembedakan beberapa karbohidrat dengan mengidentifikasi konfigurasi strukturalnya.
Glukosa dan fruktosa memberikan osazon yang sama karena kedua monosakarida tersebut memiliki gugus H dan OH yang terletak pada atom C yang sama yaitu atom C ke 3, 4 dan 5. Manosa tidak membentuk osazon melainkan membentuk fenilhidrazon yang tidak larut.
Semua disakarida kecuali sukrosa tidak membentuk osazon.
Berikut reaksi pembentukan osazon :
Reaksi Tauber
Reaksi Tauber digunakan untuk mengidentifikasi karbohidrat pentosa. Reagen Tauber berisi larutan 4 % benzidin dalam asam asetat glacial. Ketika dalam zat mengandung pentosa dan direaksikan dengan reagen Tauber, maka pentosanya akan terhidrolisis oleh asam asetat galsial menjadi senyawa furfural.Furfural yang terbentuk akan bereaksi dengan benzidin membentuk kompleks senyawa berwarna merah anggur.
Reaksi yang terjadi adalah sebagai berikut :
1. Pentosa (arabinosa) + CH3COOH glacial ==> furfural + 3H2O
∆
2. Furfural + benzidin ==> senyawa kompleks yang berwarna merah anggur
Reaksi hidrolisis sukrosa
Sukrosa jika dihidrolisis menggunakan asam dan kemudian dipanaskan akan menghasilkan dua buah molekul monosakarida. Percobaan ini bertujuan untuk membuktikan bahwa disakarida adalah gabungan dari dua buah monosakarida.Untuk melakukannya, dibutuhkan dua buah tabung reaksi. Didalam tabung reaksi ini masing-masing dimasukkan sukrosa. Kemudian dalam kedua tabung dimasukkan HCl, reagen Bennedict dan timol biru. HCl berfungsi sebagai penghidrolisis sukrosa sedangkan timol birunya berfungsi sebagai indicator.
Reagen Bennedict berfungsi sebagai penanda putusnya ikatan monosakarida dalam sukrosa. Sukrosa akan dihidrolisis menjadi fruktosa dan glukosa dimana glukosa akan bereaksi positif menghasilkan endapan merah bata. Artinya jika ada endapan merah bata maka sukrosanya telah terhidrolisis.
Tabung I akan dipanaskaskan sedangkan tabung II tidak. Tabung yang dipanaskan akan terjadi reaksi hidrolisis sukrosa sementara tabung dua tidak. Seperti yang dijelaskan diatas bahwa pada tabung I akan terbentuk endapan merah bata yang menandai telah putusnya ikatan diantara fruktosa dan glukosa yang membentuk disakarida.
Reaksi pengendapan
Untuk mengidentifikasi adanya amilum dalam suatu zat, kita bisa menggunakan reaksi pengendapan. Dalam zat akan ditambahkan ammonium sulfat jenuh ((NH4)2SO4) yang mempunytai kemampuan mengikat air.Jika ada amilum dalam zat tersebut, maka kelarutannya akan berkurang dan akhirnya mengendap. Larutan amilum dan ammonium sulfat jenuh yang dipanaskan akan menghasilkan endapan berwarna putih.
Metode ini juga bisa digunakan untuk memisahkan amilum dari larutan. Amilum yang mengendap ada dalam jumlah yang banyak, sedangkan filtratnya hanya mengandung sedikit amilum. Dengan menyaring, kita bisa mendapatkan amilum padat. Sementara amilum yang masih ada dalam flitrat dapat kita endapkan terus melalui cara diatas sampai amilumnya habis. Hal ini bisa ditandai dengan tidak terbentuknya warna biru jika filtratrnya ditetesi iod.
Reaksi hidrolisis gom arab (gummi Arabicum)
Gom arab adalah salah satu produk getah (resin) yang dihasilkan dari tanaman polog-polongan. Jika dihidrolisis, gom arab akan dipecah menjadi arabinosa (gula pentosa).Sama dengan karbohidrat lain, untuk menghidrolisis gom arab digunakan HCl dan dilakukan pemanasan. Setelah beberapa saat pemanasan, kita akan menghentikan proses hidrolisis yaitu dengan caramendinginkannya dan menambah NaOH agar suasana larutan menjadi netral.
Gula pentosa (arbinosa) yang dihasilkan dari proses hidrolisis akan bereaksi positif dengan reagen Tauber menghasilkan larutan berwarna merah. Selain itu arabinosa juga akan menghasilkan endapat merah bata yang menandai bahwa ia adalah gula pereduksi (yang memiliki gugus karbonil bebas).
Sumber :
1.Bahan ajar biokimia, poltekes bengkulu, 2011
2. Pengantar biokimia, fungsi dan struktur. Togu gultom,2001 . Fakultas pendidikan Kimia . UNY
3. Buku PR kimia kelas 12 SMA, Penerbit intan pariwara
4. Pengantar biokimia, togu gultom, fakultas pendidikan kimia, universitas yogyakarta.
Penulis: Ririn Nababan

Posting Komentar untuk "Macam Macam Cara Identifikasi Karbohidrat"